在精准抗癌的武器库中,抗体药物偶联物(ADC)犹如“生物导弹”,凭借其精准靶向和高效杀伤的特性,革新了多种癌症的治疗格局。然而,正如再先进的武器也可能遭遇防御壁垒,ADC在临床应用中,正面临着“耐药”这一严峻挑战。近期,发表于Journal of Hematology & Oncology杂志的一项重磅综述,系统梳理了ADC耐药的复杂机制,并为我们勾勒出克服耐药的前沿战略蓝图。

ADC的辉煌与困境:为何“导弹”会失效?
ADC由抗体、连接子和细胞毒性载荷三部分精巧构成。它通过抗体精准识别肿瘤细胞表面的抗原,内化后释放超强毒性的载荷,从而杀死肿瘤细胞,甚至能产生“旁观者效应”清除邻近的抗原阴性细胞。
自2000年首个ADC药物吉妥珠单抗奥佐米星获批以来,已有超过20款ADC药物应用于血液肿瘤和实体瘤,如靶向CD30的维布妥昔单抗、靶向HER2的T-DM1和DS-8201等,不断刷新着患者的生存期。
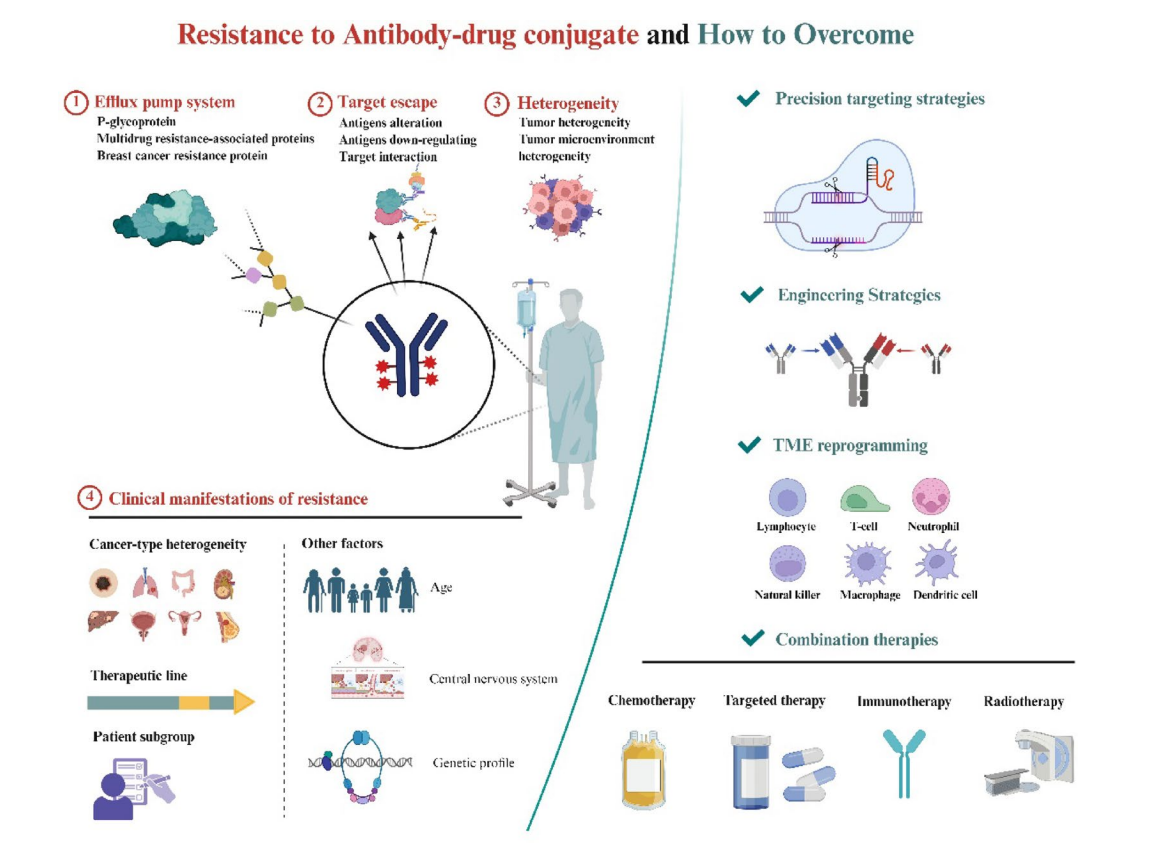
图:ADC耐药的关键分子机制及其临床表现,并总结了克服耐药、提升ADC疗效的新兴解决方案
然而,耐药性的出现成为悬在ADC疗法之上的“达摩克利斯之剑”。其耐药机制复杂多元,主要体现在四个方面:
外排泵系统:肿瘤细胞表面的P-糖蛋白、多药耐药相关蛋白和乳腺癌耐药蛋白等转运蛋白,能像“水泵”一样将ADC的有效载荷(如MMAE、DM1)主动排出细胞外,导致细胞内药物浓度不足。例如,P-gp过表达会削弱T-DM1和DS-8201的疗效。
靶点逃逸:肿瘤细胞通过使靶抗原发生突变、表达量下调或内化过程异常,来逃避ADC的识别和攻击。例如,TROP2基因突变会导致戈沙妥珠单抗耐药,CD30下调与维布妥昔单抗耐药相关,而EGFR的高表达则会通过与HER2形成二聚体,抑制DS-8201的内吞。
肿瘤异质性:同一肿瘤内部或不同转移灶之间,靶抗原的表达分布可能极不均匀。这种“斑片状”表达(如CLDN18.2在胃癌中的表达)使得ADC无法有效覆盖所有肿瘤细胞,残留的细胞亚群最终导致疾病进展。
肿瘤微环境作祟:肿瘤内部高压、致密的细胞外基质如同“铜墙铁壁”,阻碍ADC的渗透;免疫抑制细胞和缺氧环境则会进一步削弱ADC的杀伤效果,甚至诱导耐药。
耐药临床表现:因人、因病、因治疗线数而异
耐药的临床表现极具复杂性。首先,癌种差异显著:同为HER2靶向ADC,T-DM1在乳腺癌中表现卓越,但在胃癌中疗效却大打折扣;DS-8201在不同癌种中的无进展生存期也存在巨大差异。其次,治疗线数影响深远:随着治疗线数后移,ADC的疗效往往呈现下降趋势,例如恩福妥单抗和戈沙妥珠单抗在晚期线治疗中的生存获益均不及前线。再者,患者亚组是关键变量:HER2表达水平、是否合并特定驱动基因突变、既往免疫治疗反应等,都深刻影响着ADC的最终疗效。
突破耐药:从“精准升级”到“协同作战”
面对复杂的耐药网络,科学家们正在从多个维度寻求破局之道:
1,精准靶向策略升级:
表观遗传调控:使用地西他滨等药物,通过去DNA甲基化“唤醒”被沉默的肿瘤抗原,增强ADC的结合与内化。
双特异性/双靶点ADC:这类新一代ADC能同时结合同一抗原的不同表位或两个不同抗原,促进更高效的内吞,并克服因单个抗原丢失或异质性导致的耐药。例如,靶向HER2/HER3或EGFR/c-MET的双特异性ADC已在临床试验中展现出潜力。
2,工程技术精益求精:
新型载荷开发:研发能规避外排泵识别的新载荷(如OBI-992采用的依沙替康),或作用机制独特的载荷(如靶向RNA聚合酶的鹅膏蕈碱、RNA剪接抑制剂),从根源上绕过传统耐药通路。
智能递送系统:通过改造抗体,使其能同时靶向肿瘤抗原和溶酶体蛋白(如CD63),改善内吞和胞内运输效率,确保载荷精准送达“目的地”。
3,改造肿瘤微环境:
通过靶向CAF、降解透明质酸、抑制HIF-1α或使用ROCK抑制剂等手段,降低肿瘤间质压力,改善血管功能,逆转免疫抑制状态,从而为ADC的输送和发挥作用扫清障碍。
免疫刺激抗体偶联物:将ADC与TLR或STING激动剂等免疫刺激分子结合,在杀伤肿瘤细胞的同时,原位激活抗肿瘤免疫应答,将“冷肿瘤”转化为“热肿瘤”。
4,理性联合治疗:
将ADC与其他作用机制的药物联用,是克服耐药最直接的临床策略。
与靶向药联用:T-DM1联合图卡替尼,能有效克服HER2阳性乳腺癌,尤其脑转移患者的耐药。
与免疫检查点抑制剂联用:DS-8201联合帕博利珠单抗,在HER2高表达和低表达的乳腺癌中均显示出高缓解率。恩福妥单抗联合帕博利珠单抗在尿路上皮癌的一线治疗中取得了超过26个月的中位总生存期,结果令人振奋。
双ADC组合:甚至出现了戈沙妥珠单抗与恩福妥单抗联合治疗尿路上皮癌的探索,初步数据显示协同作用,为终极耐药提供了新思路。
总结与展望
ADC的耐药是一场肿瘤与人类智慧的复杂博弈。这篇综述清晰地告诉我们,未来的方向绝非单一技术的突破,而是一个多维度的精准进化:通过深度解析耐药机制,利用表观遗传学、蛋白质工程、免疫学等多学科工具,不断优化ADC本身的设计;同时,基于生物标志物,理性设计与靶向药、免疫治疗等的联合方案,为每一位患者量身定制治疗策略。
随着对耐药机制认知的不断深入和前沿技术的飞速发展,我们相信,ADC这枚“生物导弹”必将变得更加智能、精准和强大,为更多癌症患者带来持久生存的希望。
原始出处
Zhou, K., Liu, X. & Zhu, H. Overcoming resistance to antibody-drug conjugates: from mechanistic insights to cutting-edge strategies. J Hematol Oncol 18, 96 (2025). https://doi.org/10.1186/s13045-025-01752-9
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
























