嗜酸性粒细胞性食管炎(EoE)是一种慢性、免疫介导的食管疾病,以食管上皮层嗜酸性粒细胞浸润为主要特征,临床常表现为吞咽困难、食物嵌顿等症状。近年来,其发病率在西方国家持续上升,尤其在儿童和成人中已成为吞咽障碍的主要病因之一。尽管饮食消除疗法被公认为EoE治疗的基石,但如何精准识别致病食物并避免不必要的营养限制,一直是临床实践中的难点。

在这一背景下,成分解析诊断(CRD) 作为分子过敏诊断的重要工具,逐渐走入临床视野。不同于传统的皮肤点刺试验(SPT)或血清特异性IgE检测,CRD能够识别患者对特定过敏原蛋白成分的免疫反应,而非仅针对粗提取物。这一进步使得区分真正的食物过敏与交叉反应成为可能,从而为个性化饮食干预提供了新路径。
饮食疗法的“三重阶梯”:从元素饮食到精准排除
目前,EoE的饮食干预策略可分为三类:元素饮食、经验性多食物消除饮食和检测指导的饮食。研究显示,其疗效呈明显梯度分布:
-
元素饮食 虽然组织学缓解率最高(可达90%–96%),但因口感差、社会接受度低,长期依从性较差;
-
经验性六食物消除饮食(SFED) 缓解率约为50%–80%,在疗效与可行性之间取得平衡,已成为临床主流;
-
检测指导的饮食 缓解率波动较大,约在39%–66%之间,其预测准确性仍逊于前两者。
值得关注的是,近年来兴起的“阶梯式”饮食策略,如从单一食物(如仅排除牛奶)开始,逐步升级至多食物排除,不仅累积缓解率可达79%,也显著提升了患者的生活质量与依从性。
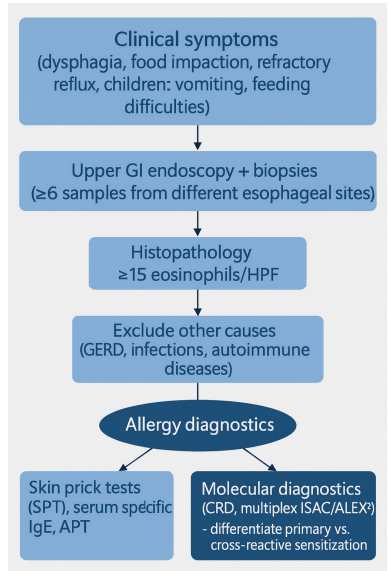
图:EoE诊断流程
CRD的优势:从“盲目排除”到“精准靶向”
尽管传统过敏检测方法在EoE中的应用效果有限,CRD却展现出独特的诊断价值。例如,Armentia等人开展的研究显示,CRD可在87.6%的EoE患者中识别出特异性过敏成分,其指导下的饮食干预使75.2%的患者症状明显改善。
CRD的核心优势在于其能够识别如脂质转移蛋白(LTP)、PR-10蛋白、原肌球蛋白等交叉反应成分,从而避免因“泛敏感”而导致的过度饮食限制。此外,结合IgG4检测、T细胞免疫分析等多维免疫指标,CRD有望构建更全面的个体化致敏图谱。
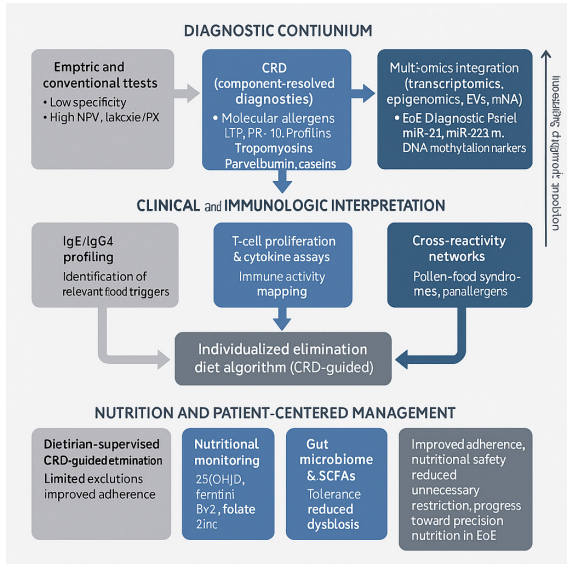
图:EoE中组分解析诊断与精准营养的整合体系
挑战仍存:CRD尚未超越经验性饮食
尽管CRD在诊断精度上有所突破,其在临床疗效上仍未显著超越经验性饮食。多项荟萃分析指出,CRD指导的饮食缓解率约为40%–65%,低于SFED和元素饮食。此外,其应用仍面临诸多限制:
-
检测成本高、平台不统一;
-
结果解读需结合临床表现与饮食史;
-
缺乏大规模前瞻性研究的验证。
换言之,CRD目前更适合作为辅助工具,而非替代现有饮食策略的“金标准”。
未来方向:多组学整合与营养安全管理
随着组学技术的发展,EoE的诊断工具有望进一步拓展。例如:
-
转录组学:EoE诊断基因面板(EDP)灵敏度高达96%;
-
表观遗传学:miR-21、miR-223等小RNA表达变化可反映疾病活动度;
-
代谢组与微生物组:揭示全身代谢状态与肠道菌群在EoE中的作用。
在推进精准医疗的同时,营养安全始终是不可忽视的一环。患者在接受长期食物排除时,易出现钙、维生素D、铁、锌等营养素缺乏。因此,CRD指导的饮食必须在营养师监督下实施,结合生化指标监测、个性化替代方案与科学的食物再引入流程,才能真正实现“疗效与安全并重”的精准营养目标。
结语
成分解析诊断代表了EoE管理从“一刀切”走向“个体化”的重要迈进。尽管目前其临床地位仍属辅助,但随着多组学数据的整合、标准化平台的建立以及营养干预路径的完善,我们有理由相信,未来的EoE治疗将更加精准、可持续,并真正体现“以患者为中心”的医疗理念。精准,不只是技术,更是对每一个患者生命质量的尊重。
原始出处
Wawrzeńczyk, A.; Napiórkowska-Baran, K.; Szota, M.; Treichel, P.; Durślewicz, J.; Bartuzi, Z. Dietary Management of Eosinophilic Esophagitis in the Era of Molecular Diagnostics: The Role and Limitations of Component-Resolved Diagnostics—A Narrative Review. Nutrients 2025, 17, 3588. https://doi.org/10.3390/nu17223588
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
























